- “Đột biến gen mthfr 677, 1298 có thai được ko?”. Câu hỏi của bạn ThuyFpt có địa chỉ email: [email protected] gửi về nhờ bộ phận tư vấn của Cty dược Poly Pharm. Khá trùng hợp câu hỏi này cũng được nhiều bạn thắc mắc. Vì vậy chúng tôi đã viết một khá cụ thể giúp bạn có thể tham khảo về vấn đề giữa gen Mthfr và mang thai.
- Chúng ta sẽ đi tìm hiểu 1 trường hợp điển hình tại MỸ. Các bác sĩ, nhà khoa học sử dụng thực tế 5-MTHF như thế nào đối với các bệnh nhân. Đặc biệt với các bệnh nhân hay sảy ra tình trạng lưu thai và đang sử dụng IVF, IUI.
- Tính khoa học của bài viết được đăng trên tạp trí ý khoa được công nhận Springer.com. Mọi điều trị của các bác sĩ, nhà khoa học tại Mỹ đều được ghi lại và theo dõi. Sau đó họ sẽ đưa vấn đề ra hội đồng y khoa. Nếu nghiên cứu đó khả thi, nghiên sẽ được công bố trên tạp trí và chúng được biết đến với tên: “BÁO CÁO DỊCH TỄ MÔ TẢ.”
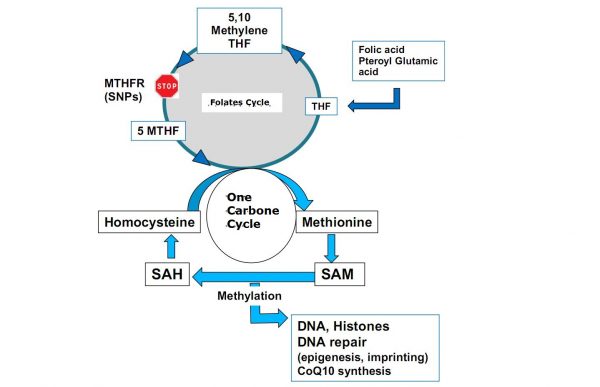
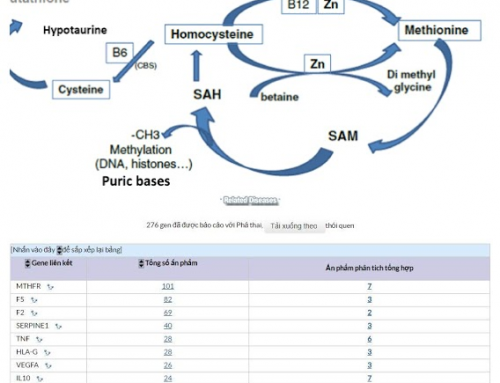
Quá trình Methyl hóa
- Quá trình Methyl hóa (quá trình thêm nhóm Methyl vào ADN) phổ biến trong quá trình quy định hóa sinh của tế bào. Nó liên quan đến phản ứng miễn dịch, chức năng dẫn truyền thần kinh, vận chuyển qua màng và sửa chữa ADN.
- Nó cũng đóng một vai trò bắt buộc trong điều hòa và bất hoạt biểu hiện gen qua in dấu và biểu sinh gen (là 2 quá trình phụ thuộc hoàn toàn vào quá trình methyl hóa ADN và các Histones). Hai quy định hóa sinh này có tầm quan trọng lớn trong quá trình tạo giao từ và phát triển phôi sớm.
- Chu trình folate là một hỗ trợ quan trọng trong quá trình Methyl hóa. Nó cho phép tái methionine từ quá trình methyl hóa homocysteine thông qua SAM (S Adenosyl Methionine).
- MTHFR là tác nhân mạnh mẽ của chu trình folate. Nhưng các biến thể di truyền (677CT và 1298AC) làm giảm hoạt động enzyme. Bên cạnh việc liên quan đến các vấn đề về tuần hoàn máu, tim mạch và ung thư. Các biến thể này còn có mối tương quan chặt chẽ với sự suy giảm chức năng sinh sản bao gồm phát sinh giao tử đực, phát sinh phôi giai đoạn sớm và muộn, phát triển và cấy ghép nguyên bào nuôi phôi và có thể liên quan đến sảy thai tái phát (RPL).
Đột biến gen MTHFR 677CT & A1298C là gì đọc thêm >>Tại Đây<<
- Trong bài viết sẽ có ký hiệu viết tắt NHL (U Lympho không Hodgkin) cũng có mối tương quan chặt chẽ với MTHFR.
Mang thai đột biến gen MTHFR 677CT
- Bệnh nhân 34 tuổi, vào thời điểm 3/2017. Khởi phát kinh nguyện của bệnh nhân vào 3/1995. Tiền sử uống thuốc tránh thai từ năm 2000 – 2014. Cô bị sảy thai lần đầu vào 6/2015 khi mang thai 12 tuần và sau khi được bổ sung vitamin dài ngày với axit folic.
- Bệnh nhân ngừng sử dụng vitamin này khi cô được chẩn đoán mắc U lympho không Hodgkin, vào 7/2015.
- Giai đoạn 8/2015 – 12/2015 bệnh nhân được điều trị bằng sự kết hợp của các loại thuốc R-EPOCH (bao gồm Rituximab, Etoposide phosphate, Prednison, Vincristine sulfate (Oncovin), Cyclophosphamide và Hydroxydaunorubicin). Cùng lúc trải qua hóa trị, cô cũng được điều trị bằng chất chủ vận LHRH.
Ảnh: Đột biến gen MTHFR 677CT
Sau khi thuyên giảm NHL
- Các vitamin trước khi sinh chứa axit folic đã được sử dụng lại.
- Cô bị sảy thai lần thứ hai vào tháng 10 năm 2016, lúc 7 tuần tuổi thai.
Phỏng đoán đầu tiên
- Vào ngày 2 tháng 3 năm 2017, cô ấy đã có phỏng đoán đầu tiên:
- Xét nghiệm thấy giá trị AMH ở mức 0,007 nG / mL.
- Siêu âm vùng chậu cho thấy buồng trứng phì đại với một u nang chức năng ở buồng trứng phải đo được kích thước 20mm. Sau đó là 24 mm và không có nang trứng, nhưng tử cung có kích thước bình thường.
- Buồng trứng bên trái bị teo nhỏ với thể tích 1,91 mL và hai nang noãn. 2 bên ống dẫn trống.
- Bệnh nhân được chẩn đoán bị suy buồng trứng sớm và cặp vợ chồng được tư vấn sử dụng DHEA 25 mg ba lần một ngày.
Tháng 4/2017
- Xét nghiệm thân nhiệt chuẩn (BBT) cho thấy giai đoạn hoàng thể rất ngắn 6-7 ngày.
- Ngày 19/4, estradiol là 287 ɳG / L và progesterone ở mức 3,13 μG / L.
- Vào tháng 9/2017, AMH luôn ở mức thấp: <0,003 và bệnh nhân được phát hiện đồng hợp tử MTHFR C677T với nồng độ homocysteine huyết tương ở mức bình thường (9,1 μ mol / L).
- Bệnh nhân được yêu cầu ngừng tất cả các Thực phẩm chức năng chứa axit folic và bắt đầu sử dụng Methyl Folate 800mg mỗi ngày và phức hợp Vitamin B và B12.
3 tháng sau, bệnh nhân có thai.
- Tháng 11/2017, khi thai được 5 tuần, siêu âm cho thấy sự hiện diện của hai túi tử cung với túi noãn hoàng, có đường kính túi trung bình lần lượt là 9mm và 13mm (có thể là sinh đôi).
- Tháng 12.2017. Bệnh nhân tiếp tục siêu âm và thấy chỉ còn một túi thai có túi noãn hoàng và tim thai. Chẩn đoán sinh đôi đã biến mất.
- Bệnh nhân được theo dõi cứ sau 2 tuần bắt đầu từ 32 tuần tuổi thai, nhưng ở tuần thai thứ 36. Cô được phát hiện quá ít nước ối và mắc chứng tiền sản giật. Bệnh nhân có chỉ số AFI (chỉ số nước ối) là 4,1 và phải nhập viện để theo dõi và truyền dịch qua tĩnh mạch.
- Tuần 37. Một bé trai khỏe mạnh 2,69 kg đã được sinh ra. Bệnh nhân cho con bú và được khuyên nên tiếp tục dùng 5-MTHF và phức hợp vitamin B.
Thảo luận, kết luận.
- Báo cáo trường hợp này phù hợp với sự xuất hiện của mối liên quan giữa phá thai thường xuyên và đột biến MTHFR. Sự xuất hiện NHL ở bệnh nhân dường như cũng liên quan đến MTHFR vì chúng ảnh hưởng đến quá trình tạo giao tử âm, sự phát triển phôi sớm và muộn.
Đọc thêm về đột biến gen MTHFR nguy cơ cần biết >>Tại Đây<<
Ảnh:Gen MTHFR hiện đang đứng đầu về tỉ lệ sảy thai lặp lại
- Điều này cũng có nghĩa là bệnh nhân nên được kiểm tra đột biến MTHFR. Có thể trước khi được hiến tế bào trứng. Theo quan sát, phương pháp xét nghiệm mức homocysteine được đánh giá yếu hơn vì giá trị của nó không nhất thiết tương quan với nền tảng di truyền MTHFR.
- Một số chất mang có thể được chuyển hóa (homocysteine bình thường) trong điều kiện tiêu chuẩn nhưng có thể trải qua sự mất cân bằng bệnh lý tại thời điểm nhu cầu trao đổi chất tăng lên. Vì đó là trường hợp phát triển giao tử và phát triển phôi.
Axit folic liều cao thực sự là một vấn đề.
- Axit folic tổng hợp (Pteroyl Glutamic acid) ít có khả năng để đi vào chu trình folate để tạo thành Tetrahyydrofolate (THF) và sau đó 5-MTHF là hợp chất cần thiết hoạt động tái tạo Homocysteine.
- Điều này dẫn đến sự xuất hiện của UMFA. Hội chứng không chuyển hóa được axit folic. Điều này có thể tác động rất tiêu cực như xuất hiện một số khối u (đại trực tràng, tuyến tiền liệt).
Báo cáo này xem xét trường hợp của một bệnh nhân nữ bị sảy thai tái phát (RPL(Sảy thai liên tiếp)) và suy buồng trứng sớm sau khi điều trị NHL. Sau khi phát hiện đột biến đồng hợp tử gen MTHFR 677CT. Bệnh nhân đã được điều trị thành công với 5-MTHF và sinh được một bé trai khỏe mạnh.
Kết quả nghiên cứu công bố
- Phương pháp điều trị với sự hỗ trợ của một chu trình carbon có thể cải thiện chất lượng buồng trứng ở một số bệnh nhân. Vì nó cho phép cải thiện quá trình tạo giao tử. Về mặt này, 5-MTHF là một công cụ hữu ích với các vấn đề phụ thuộc vào sự thiếu hụt MTHFR.
- 5-MTHF cho phép vượt qua enzyme bị đột biến và tránh các vấn đề từ liều cao của axit folic tổng hợp có thể gây ra sự xuất hiện của hội chứng UMFA và pseudo MTHFR (ức chế một chu trình carbon do sự cạnh tranh của axit folic cung cấp với tiền chất tự nhiên của 5-MTHF).
- Liều cao của axit folic thực sự có thể gây ra sự gia tăng homocysteine: Nó không phải là một lựa chọn điều trị tốt.
Xét nghiệm chính xác MTHFR trên bệnh nhân. Sau đó là điều trị với 5-MTHF, có thể giúp tránh được nhu cầu sàng lọc di truyền trước cấy ghép, thủ thuật cấy ghép tốn kém. Được cho là để khắc phục sảy thai không rõ nguyên nhân.
Kết luận
- Qua chứng minh lâm sàng vừa rồi chúng ta thấy tầm quan trọng của việc sử dụng 5-MTHF đối với người có đột biến gen MTHFR và bạn hoàn toàn mang thai được với gen MTHFR (cụ thể ở đây là dạng MTHFR 677CT).
- Tỉ lệ đột biến gen khá cao khoảng 30-52%, tức là cứ 10 ngưới sẽ có 3-5 người bị đột biến gen này. Tại Việt Nam chưa có thống kê nhưng tỉ lệ được dự báo cáo hơn nhiều so với các nước như MỸ, Canada..Đó là lí do tại sao ngày càng có nhiều trường hợp vô sinh, khó sinh, lưu thai…
- Giải pháp đó là sử dụng 5-MTHF trong quá trình này để giải quyết vấn đề về đột biến gen, lưu thai, sảy thai được cho là một bước đi đầy triển vọng trong việc mang thai.
https://doi.org/10.1007/s10815-018-1332-0




Gửi bình luận